虽然基因编辑技术进步显著,但人类已识别的超过七万五千种与疾病相关的基因变异里[1],很大一部分在涉及治疗的细胞类型中仍难以修正。对于多数遗传病,要想深入研究或治疗其根本原因,关键在于精确修正特定基因的突变,而非对基因进行无目的的破坏。然而,当前Cas9介导的同源重组(HDR)技术修复效率尚不尽人意。有鉴于此,哈佛大学的David Liu教授开创了一系列新颖的碱基编辑技术,包括胞嘧啶编辑器(CBE,实现C→T或G→A的转换)、腺嘌呤编辑器(ABE,实现A→G或T→C的转换)以及更为先进的先导编辑器(PE,能修复高达89%的人类致病突变)[2,3]。David Liu教授凭借这些突破性成就,近期荣获美国科学院院士的殊荣。
遗传性酪氨酸血症I型(HT1),亦称作先天性酪氨酸血症,属于遗传性基因突变疾病的一种。这种病症是由于富马醛乙酰丙酮酶(FAH)基因的第8个外显子末端发生了G到A的突变,从而导致在剪切过程中跳过了Exon8,使得FAH失活。FAH的缺乏会导致酪氨酸代谢异常,引发严重的肝损伤和肾小管缺陷,进而可能诱发肝纤维化、肝硬化,甚至肝癌。
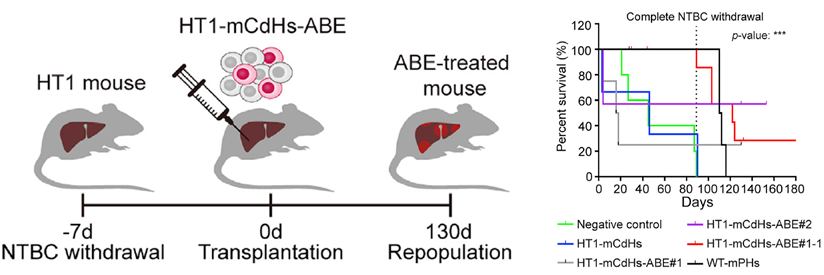
2021年5月4日,韩国汉阳大学的Dongho Choi教授在《Cell Stem Cell》期刊上发表了一篇题为“Adenine base editing and prime editing of chemically derived hepatic progenitors rescue genetic liver disease”的论文。在这项研究中,Choi教授利用腺嘌呤碱基编辑(ABE)和先导编辑(PE)技术对通过化学方法获得的肝祖细胞进行体外编辑,并将编辑后的细胞再移植到小鼠体内,成功治疗了遗传性肝脏疾病。
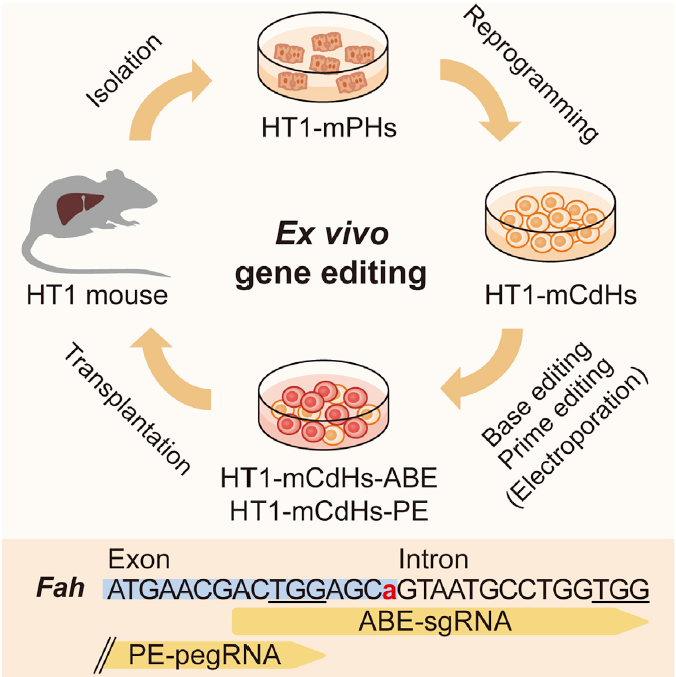
遗传性酪氨酸血症I型(HT1)是一种由富马醛乙酰丙酮酶(FAH)缺乏导致的常染色体隐性遗传病,这种疾病可能会引发肝癌(HCC)。尽管使用NTBC药物治疗HT1可以产生一定的疗效,但有些患者对NTBC并不敏感,并且在治疗过程中仍然存在发展为肝癌的风险[4]。研究者们已经尝试通过基因编辑技术对FAH基因或其他相关基因进行体内编辑,并取得了一定的进展。体内编辑策略具有一些优势,但在临床应用方面也面临一些挑战,包括难以精确控制CRISPR相关工具的传递剂量,以及无法筛选出正确编辑的细胞,以排除发生无关突变或脱靶效应的细胞。相比之下,离体编辑策略可以有效克服这些难题,并且能够避免可能的免疫反应等不适应症状[5]。在这项研究中,作者采用了之前开发的化学衍生肝祖细胞(chemically derived hepatic progenitors, CdHs)方法来获取HT1小鼠的肝祖细胞(mCdHs)[6],并使用这些细胞进行离体基因编辑治疗。
1、HT1小鼠的CdHs细胞的生成和表征
为了生成HT1模型小鼠的mCdHs细胞,研究者们采用了之前开发的技术来处理小鼠的原代肝细胞(mPHs),这一过程被称为肝细胞转化为肝祖细胞(HAC)。经过HAC处理的细胞开始表达肝祖细胞特有的标志物,例如Krt19、Sox9和Afp。通过对这些细胞进行RNA测序分析,研究结果显示HT1-mCdHs细胞的转录组与原始的HT1-mPHs细胞存在显著差异,尤其是在细胞周期相关基因的表达方面,HT1-mCdHs细胞显示出显著的上调。肝祖细胞在体内具有分化为成熟肝细胞和胆管细胞的能力,而作者观察到即使在稳定传代23次之后,HT1-mCdHs细胞仍然保留着向这两种细胞类型分化的潜力。
2、突变的HT1小鼠的CdHs细胞可以利用BE和PE成功纠正
随后,研究者们着手开发一种精确的基因编辑方法,旨在纠正HT1-mCdHs细胞中的Fah基因第八个外显子的G>A点突变。在尝试了多种腺嘌呤碱基编辑(ABE)方法后,发现NG-ABE8e方法在编辑效率上表现最佳,最终达到了9.2%的编辑效率。然而,该方法也导致了邻近区域两个A碱基的编辑,编辑率分别为12.4%和11%。在经过一系列优化后,先导编辑(PE)方法实现了2.3%的编辑效率,且没有观察到邻近区域的编辑效应。
接着,作者对正确编辑的HT1-mCdHs细胞系进行了稀释分离,得到了ABE#1和ABE#2细胞系。遗憾的是,由于小鼠肝细胞的多倍体特性,即使对ABE#1进行了再次稀释,也没有能够获得纯合子细胞系。通过高通量测序对ABE#1-1细胞系进行评估,发现其纠正率为13.1%,并且没有检测到明显的脱靶效应。
3、被编辑纠正的HT1小鼠的mCdHs细胞可以在肝脏再生并延长HT1小鼠存活天数
为了验证编辑后的mCdHs细胞是否能在HT1小鼠体内实现再生,研究者将部分编辑过的HT1-mCdHs-ABE细胞系移植到HT1小鼠体内。实验结果表明,接受移植的小鼠肝脏损伤程度有所减轻,肝脏切片中出现了Fah阳性组织,并且小鼠的寿命显著延长。这些发现表明,编辑后的mCdHs细胞在小鼠体内具有显著的再生和分化能力,这种离体基因编辑策略有望治疗HT1小鼠的遗传性肝病。
由于PE编辑细胞群显示出足够的编辑效率(2.3%)且没有邻近编辑效应,研究者直接将PE编辑后的细胞群移植到小鼠体内。实验结果与ABE编辑细胞系的移植结果相似,进一步证明了这种基因编辑策略的有效性。
总结来说,研究者们开发的离体基因编辑mCdHs策略具有以下几个显著优势:
- 不需要引入可能改变基因的外源因子;
- 在移植前可以对编辑效率和脱靶效应进行评估和筛选;
- 由于可以在体外对细胞系进行富集,编辑效率的要求不像体内编辑那样严格,而且使用电转化的方式相对于病毒载体来说更为方便和安全。
Reference
Search-and-replace genome editing without double-strand breaks or donor DNA. Anzalone, A.V.; Randolph, P.B.; Davis, J.R.; Sousa, A.A.; Koblan, L.W.; Levy, J.M.; Chen, P.J.; Wilson, C.; Newby, G.A.; Raguram, A.; Liu, D.R. Nature, 576, 149–157 (2019)
Programmable Editing of a Target Base in Genomic DNA Without Double-Stranded DNA Cleavage. Komor, A. C.; Kim, Y. B.; Packer, M. S.; Zuris, J. A.; Liu, D. R. Nature 533, 420-424 (2016).
Programmable Base Editing of A•T to G•C in Genomic DNA Without DNA Cleavage. Gaudelli, N. M.; Komor, A. C.; Rees, H. A.; Packer, M. S.; Badran, A. H.; Bryson, D. I.; Liu, D. R. Nature 551, 464-471 (2017).
van Ginkel, W.G., Rodenburg, I.L., Harding, C.O., Hollak, C.E.M., Heiner-Fokkema, M.R., and van Spronsen, F.J. (2019). Long-term outcomes and practical considerations in the pharmacological management of tyrosinemia type 1. Paediatr. Drugs 21, 413–426.
Song, C.Q., Jiang, T., Richter, M., Rhym, L.H., Koblan, L.W., Zafra, M.P., Schatoff, E.M., Doman, J.L., Cao, Y., Dow, L.E., et al. (2020). Adenine base editing in an adult mouse model of tyrosinaemia. Nat. Biomed. Eng. 4, 125–130.
Crudele, J.M., and Chamberlain, J.S. (2018). Cas9 immunity creates challenges for CRISPR gene editing therapies. Nat. Commun. 9, 3497.
Kim, Y., Kang, K., Lee, S.B., Seo, D., Yoon, S., Kim, S.J., Jang, K., Jung, Y.K., Lee, K.G., Factor, V.M., et al. (2019b). Small molecule-mediated reprogramming of human hepatocytes into bipotent progenitor cells. J. Hepatol. 70, 97–107.
- 本文作者: Anderson
- 本文链接: http://nikolahuang.github.io/2021/05/04/Using-BE-and-PE-to-edit-chemically-derived-mouse-hepatic-progenitor-cells-in-vitro/
- 版权声明: 转载请注明出处,谢谢。

