SpyTag技术为蛋白赋能
2023-10-24转载
1 .摘要
本文详述了SpyTag技术的原理,及其在检测和控制蛋白活力方面的潜力。SpyTag与SpyCatcher结合时自发形成不可逆的异肽键。SpyTag/SpyCatcher具有机械稳定性,因此被广泛用于研究蛋白折叠和力敏感性。一系列支架工具允许将SpyTag融合体组装成多聚体,从二聚体到180聚体或无限的1D、2D或3D网络。对于酶来说,Spy技术提高了蛋白的韧性,促进了底物通道,并组装了连续流生物催化的水凝胶。在活细胞中,SpyTag技术允许蛋白转运的成像,CAR-T细胞杀伤的重新定位,及核小体位置的控制。
2 .原理
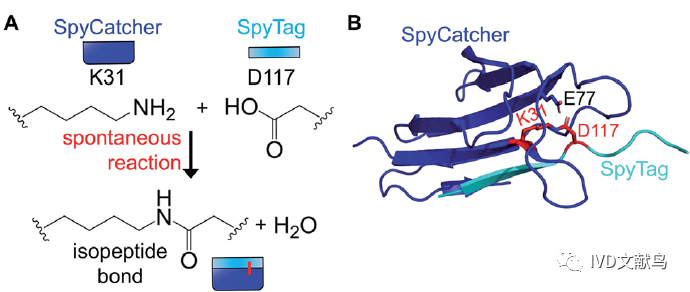
SpyTag/SpyCatcher是一种蛋白偶联方法,通过从化脓性链球菌纤维连接蛋白FbaB中分离的CnaB2结构域而产生。CnaB2自发地在Lys31和Asp117之间形成分子内异肽键(图1A)。SpyCatcher有113个氨基酸,含有活性Lys31,SpyTag,有13个氨基酸,含活性Asp117(图1A)。混合后,SpyTag和SpyCatcher结合并自发地进行由Spy-Catcher残基Glu77促进的酰胺化反应,形成分子间异肽键(图1B)。SpyTag/SpyCatcher之间的自发酰胺化发生在很宽的温度范围和pH范围。SpyTag和SpyCatcher可以融合到蛋白的N端或C端,在某些情况下也可以融合到蛋白内部的loop结构。这两个片段都不含半胱氨酸,因此很容易在不同的细胞位置使用。该反应是不可逆的,可达到99%的转化率。
3 .应用
SpyTag/SpyCatcher 亲和力改进
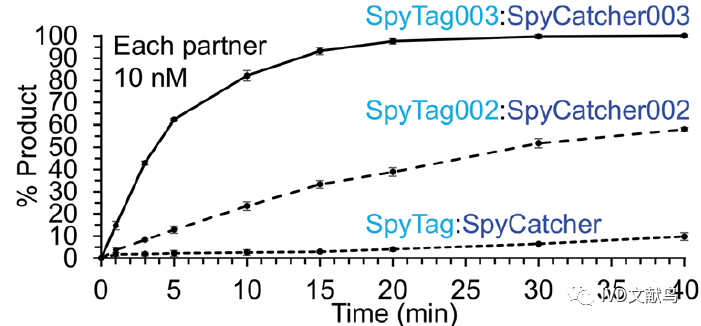
通过噬菌体展示选择和理性设计,突变体SpyTag003/SpyCatcher003具有接近无限亲和的动力学。SpyTag003/SpyCatcher003的反应速率为5.5105 M-1 s-1,比SpyTag/ SpyCatcher(1.4103 M-1 s-1)快约400倍(图2)。即使在低蛋白浓度(10 nM)下,SpyTag003/SpyCatcher003在15分钟内反应接近完成,在此条件下,原始SpyTag/SpyCatcher几乎没有反应(图2)。
Spy&Go:非反应性 SpyCatcher 亲和纯化
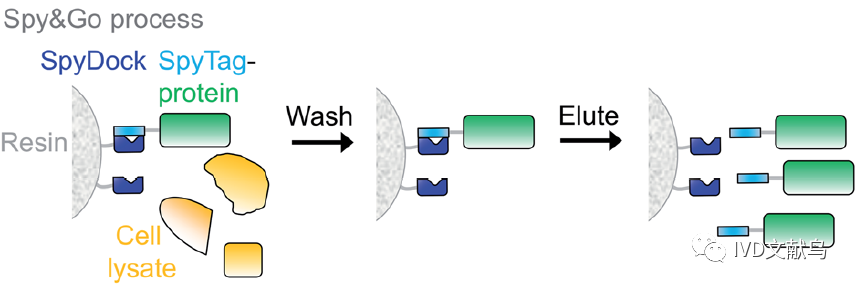
理想的纯化标签能够从复杂的混合物中简单有效地分离蛋白,但也应该增强该蛋白的下游功能。为了避免His6标签的局限性,如Ni2+的毒性,建立了使用SpyTag进行蛋白纯化的技术。Spy&Go采用无反应性SpyCatcher突变体(SpyDock),对含有反应性SpyTags(original、SpyTag002或SpyTag003)的蛋白进行纯化(图3)。用Spy&Go法纯化双标记(His6-tag/SpyTag)麦芽糖结合蛋白的纯度高于Ni-NTA纯化的纯度。Spy&Go可以从裂解物中纯化出N端或C端融合SpyTag以及内部含有SpyTag的蛋白,其结合能力为4-13 mg/毫升。SpyDock树脂可多次再生,并可在20%乙醇中保存。
锚定到微粒表面
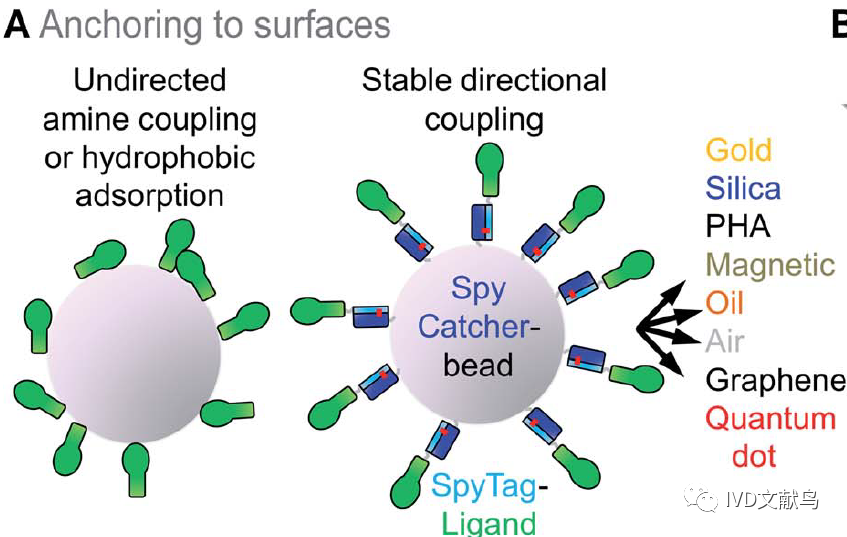
对于磁珠的连接,与羧酸激活的非特异性附着相比,SpyTag显示了定向介导的单域抗体锚定的优势(图4)。SpyTag介导的锚定已被应用于一系列蛋白的表面功能化,包括金纳米颗粒和量子点。利用SpyTag在单层石墨烯上进行锚定,可以提高低温电子显微镜在原子分辨率下的结构测定。SpyTag连接的蛋白可以固定在仿生硅组装的二氧化硅颗粒上或固定在细胞内合成的塑料颗粒上(图4)。
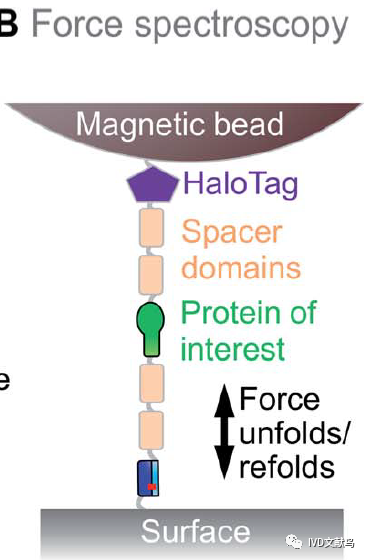
为了解决胺介导的连接的不精确性,蛋白被融合到AviTag肽上,并使用BirA进行特异性地生物素化。生物素化的蛋白可以偶联到链霉亲和素连接的表面。然而,链霉亲和素/生物素连接是可逆的,BirA可能无法使反应完全。SpyCatcher的N端的Lys和SpyTag的C端Asp间异肽键,这样力通过异肽键,而不破坏SpyCatcher结构域的其余部分。因此,SpyTag/SpyCatcher已成为力谱的常用工具(图5)。例如,这种SpyTag锚定拉伸已被用于测试人类听力的机械基础或研究设计的膜蛋白的折叠方式。SpyTag锚定后可以使用原子力显微镜,光学镊子,或磁镊子测量力。
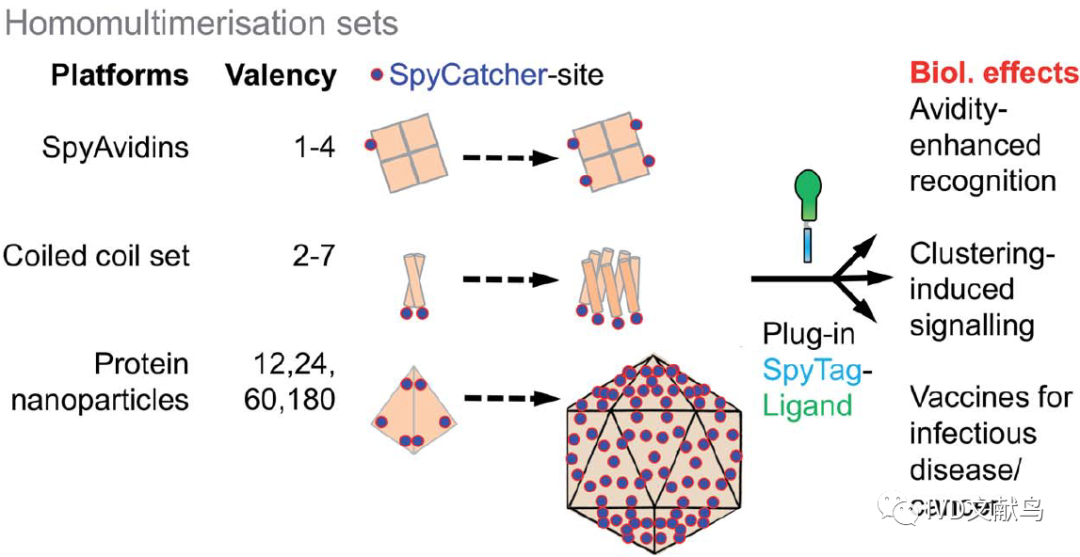
控制蛋白的聚合状态
天然蛋白有多种多聚结构,从熟悉的二聚体和四聚体,到具有60或180个拷贝的二十面体结构。这种多聚对蛋白活性产生重大影响。模块化共价组装产生一种携带SpyTag的蛋白,然后立即靠近其他蛋白支架工具箱(图6)。具有二面体对称的低聚组合可以通过“SpyAvidins”获得。研究发现链霉亲和素亚基可以与SpyCatcher融合,然后精确地用1、2、3或4个SpyCatcher拷贝产生的嵌合四聚体。因此,配体可以聚集,也可以与生物素化的配体结合。
为了获得更高的多聚体,使用了二十面体蛋白结构(图6)。与Dodecin融合的SpyCatcher是一种稳定的12聚体,可以定量地与SpyTag融合的配体偶联。SpyCatcher-linked铁蛋白有24个亚基,用于多聚化肿瘤新抗原。SpyCatcher-mi3是理性设计的60聚体,可在大肠杆菌中有效表达。SpyCatcher-AP205基于噬菌体衣壳,有180个亚基,可以与HIV、结核病和癌症相关的抗原偶联。
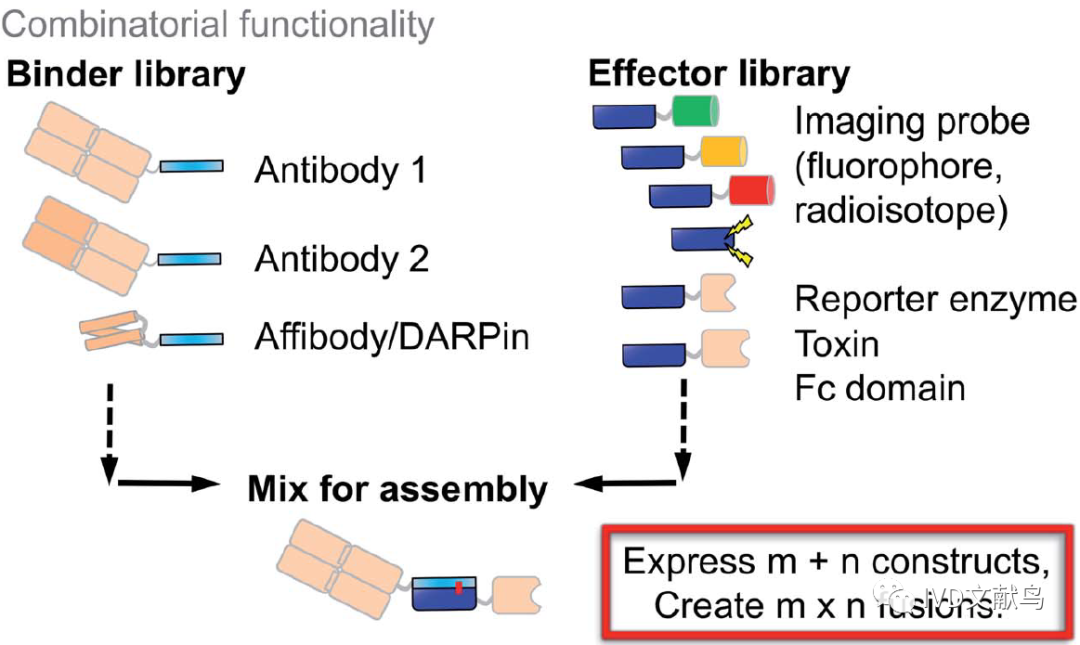
蛋白功能复合化
具有不同功能的蛋白可以通过基因融合连接在一起。然而,这样增加了蛋白折叠的复杂性。因此,有时模块化耦合更可取。人类蛋白组计划长期以来为人类蛋白组中的每种蛋白提供特定的结合试剂。共约20000种试剂,人们希望把8个不同荧光团和探针连接到每种试剂,以用于ELISA和体内成像,这是一个巨大的工程。但是,使用模块化耦合,可大大减少工作量(图7)。
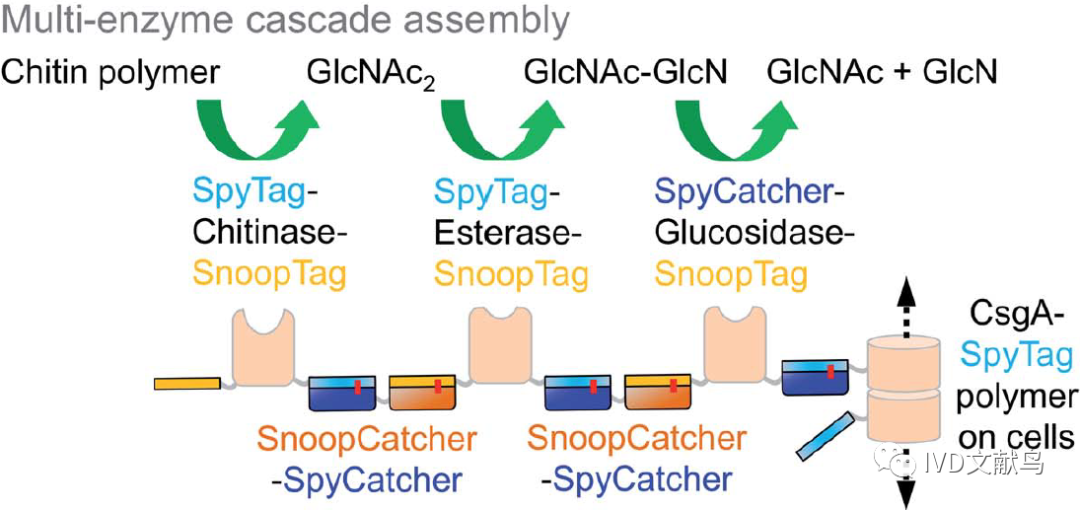
通过将SpyTag/SpyCatcher与SnoopTag/ SnoopCatcher正交结合,可以增强多组分组装,因此在Sepharose固相上应用了9个连接步骤。测试了由此产生的抗体/纳米抗体在癌症细胞杀伤中的协同作用。CsgA淀粉样蛋白也可以作为固相,用于几丁质降解多酶途径的顺序组装(图8)。
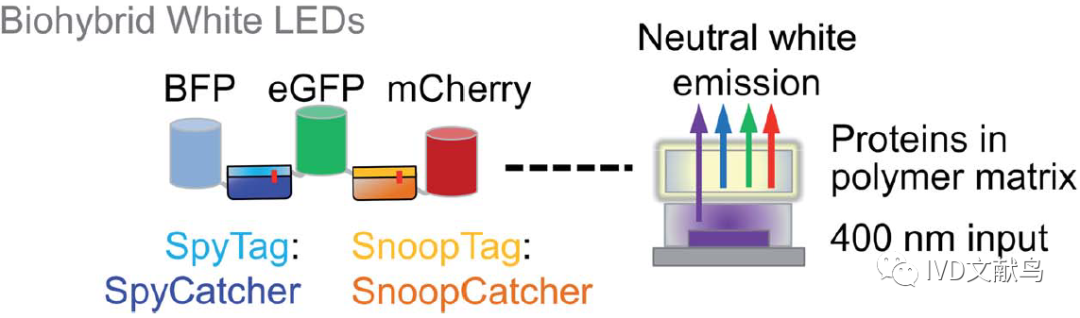
为了解决传统发光二极管荧光粉对环境的影响,通过连接不同荧光蛋白来组装白色LED(图9)。同样,为了增加太阳能的转换,植物光捕获复合体与一种紫色光合细菌的反应中心共价结合,产生互补光吸收。
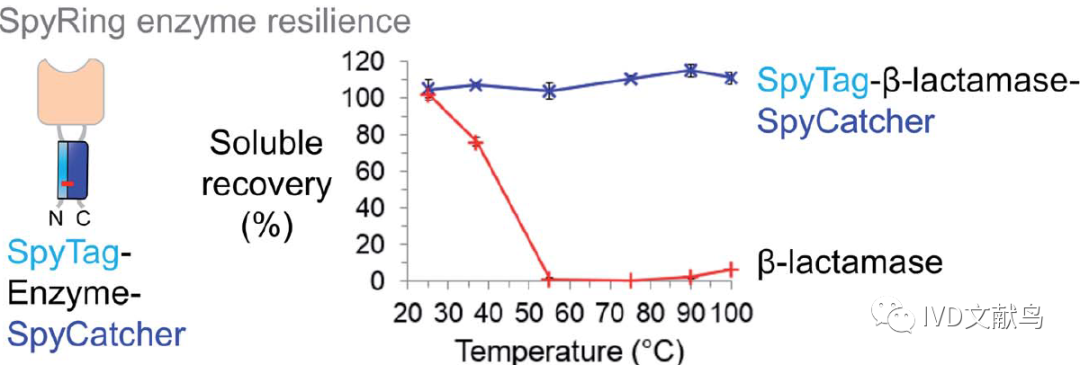
酶的弹性和组装
酶通常需要一个动态结构来结合和释放它们的底物和产物。因此,酶的稳定性在许多情况下是有限的。由于末端通常是蛋白中最灵活的部分,我们测试了如何通过SpyTag/SpyCatcher将末端锁定在一起(图10),以改变酶的弹性。研究发现,如果以这种方式环化,往往收效颇丰,如,β-内酰胺酶在沸腾后几乎保留了所有的溶解度和催化活性(图10)。除温度外,环化后对有机溶剂和变性剂的耐受性增强。
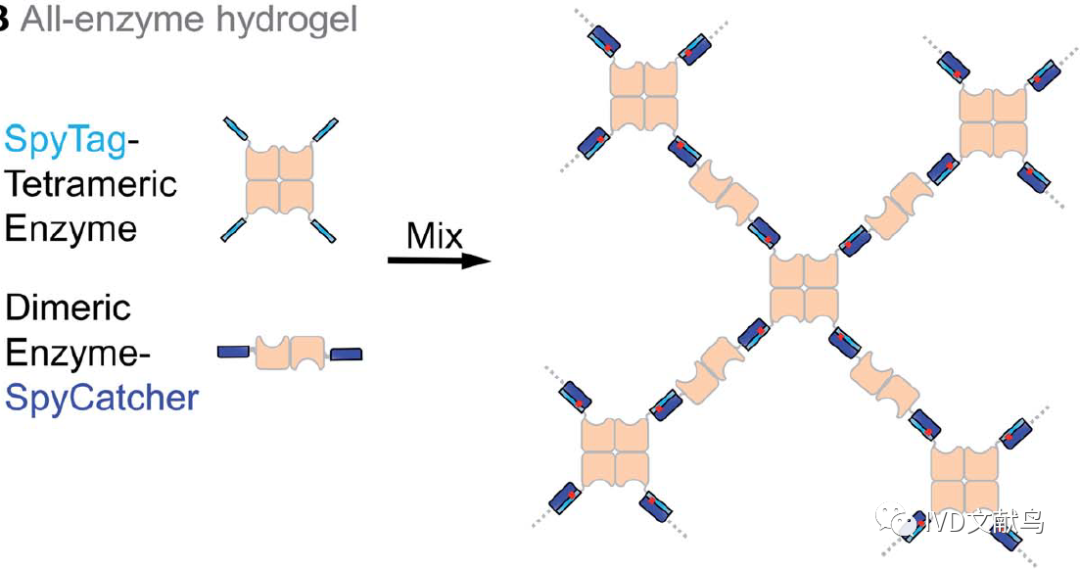
使用SpyTag/SpyCatcher与酶本身作为构建材料组装水凝胶。这些酶网络在连续流动生物催化中表现出高效的催化转化和良好的稳定性(图11)。将3种酶与SpyTag/SpyCatcher连接到弹性蛋白样多肽的水凝胶中,提高了维生素K2生物合成的产量。
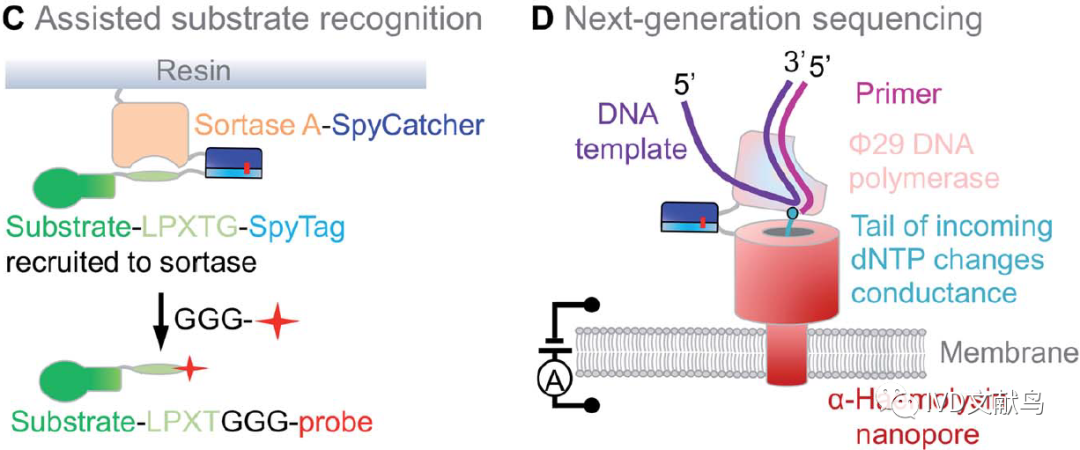
为了提高酶的性能,SpyTag/SpyCatcher可以促进底物的招募。Sortase识别底物蛋白上的–LPXTG基序,并引导连接到携带寡甘氨酸的探针(图12C)。Tsourkas使用与SpyTag连接的-LPXTG和与SpyCatcher连接的Sortase,增强了底物对接,提高了反应速度和产量(图12C)。精确定位和长期组装对于下一代DNA测序也很重要,SpyTag将DNA聚合酶定位在纳米孔附近,电流变化读出核酸序列(图12D)。
细胞生物学应用
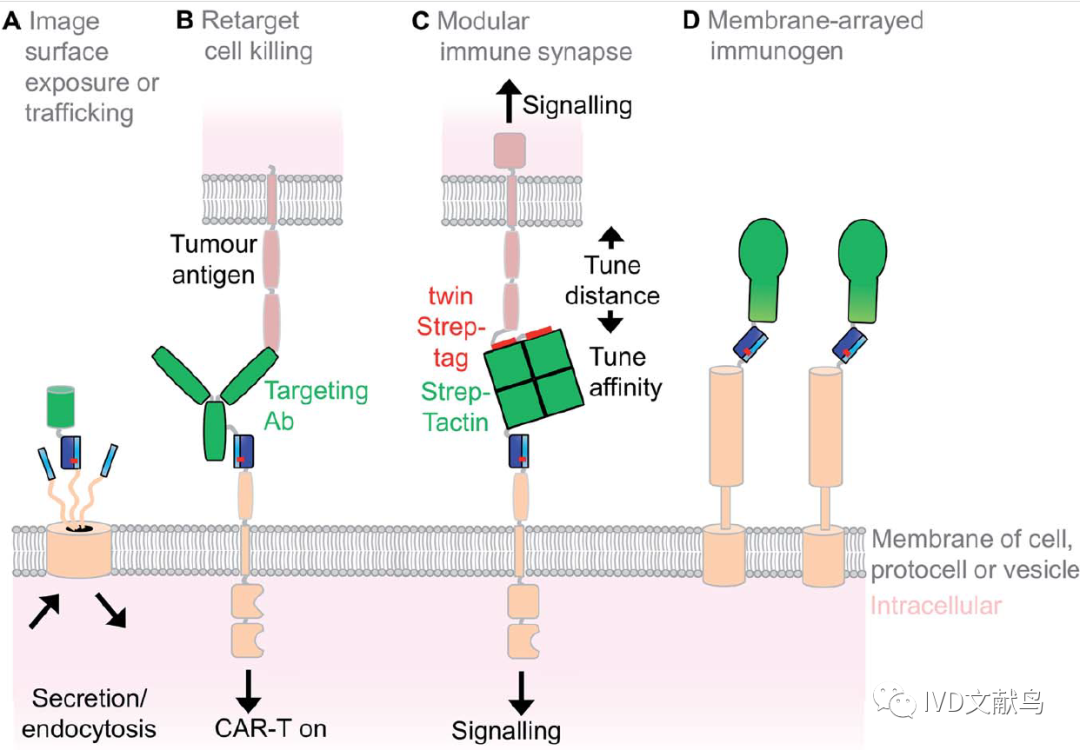
关于SpyTag的第一篇论文展示了如何使用与荧光染料连接的SpyCatcher将肽与感兴趣的细胞表面蛋白(ICAM-1)融合,用于活细胞上的特异性标记(图13A)。近年来,使用检查点抑制剂或嵌合抗原受体(CAR)T细胞的免疫疗法取得了临床成功,这是癌症治疗的一场革命。与SpyTag融合的抗体已被注射到小鼠,以引导表达SpyCatcher的CAR-T细胞杀死卵巢癌症(图13B)。为了加强对免疫系统中细胞-细胞相互作用的研究,在与质膜不同距离处存在SpyTag,以产生稳定的转染物(图13C)。膜修饰也可用于疫苗组装:减毒沙门氏菌的外膜囊泡含有SpyTag连接的大肠杆菌自身转运子,有助于展示SpyCatcher连接的免疫原(图13D)。
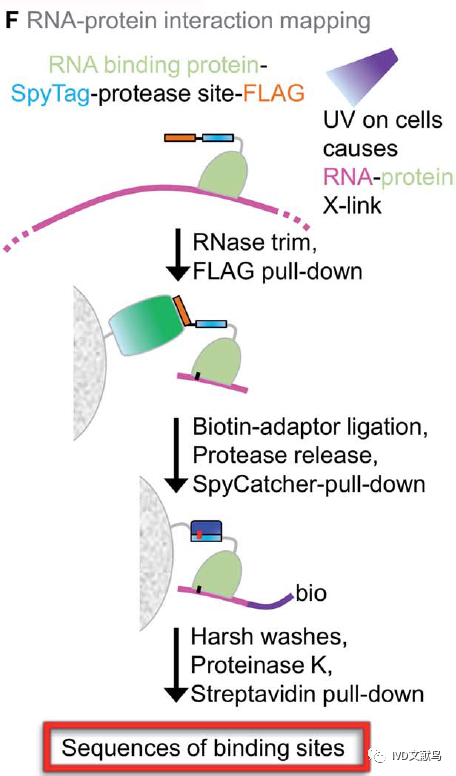
SpyTag技术已应用于各种遗传和表观遗传研究。SpyCLIP被开发用于绘制细胞中RNA-蛋白相互作用,利用不可逆的SpyTag相互作用来减少背景并提高下拉效率(图14)。在细胞核内,SpyTag已被融合到转录因子中,用于改变核小体定位(图15)或用于CRISPR介导的基因编辑的缩小版Cas9。

4 .结论
像电子电路板中的组件一样可靠地重定向生物单元,是合成生物学的目标。拥有简单可靠的方法来连接蛋白之间或非蛋白成分是实现这一目标的重要组成部分。本文介绍了如何找到许多方法来使用SpyTag来应对这些挑战。SpyTag现在可以在蛋白生命的每个阶段做出贡献:纯化,分析和在细胞上或离体上的应用。
5 .文章信息
期刊:Chemical Science
DOI:10.1039/D0SC01878C
https://pubmed.ncbi.nlm.nih.gov/33552459/
- 本文作者: Anderson
- 本文链接: http://nikolahuang.github.io/2023/10/24/SpyTag技术为蛋白赋能/
- 版权声明: 转载请注明出处,谢谢。

